IMMUNITÀ: Decifrano il percorso che ci aiuta a produrre i nostri anticorpi

Il nostro corpo produce costantemente anticorpi specifici, destinati a combattere gli invasori patogeni, come virus o allergeni. Questo team dell’Università di Augusta (Georgia) ha scoperto il modo in cui la loro produzione è alimentata e mantenuta. Questi lavori presentati sulla rivista Nature Communications aprono la speranza di poter un giorno essere in grado di regolare questo percorso di immunità, per mantenerci in salute.
È un meccanismo protettivo essenziale che resta da capire meglio, specifica l’autore principale, lo scienziato Nagendra Singh, immunologo nel dipartimento di biochimica e biologia di Augusta: “Stiamo cercando di progettare piccole molecole in grado di bloccare o per attivare questo canale “.
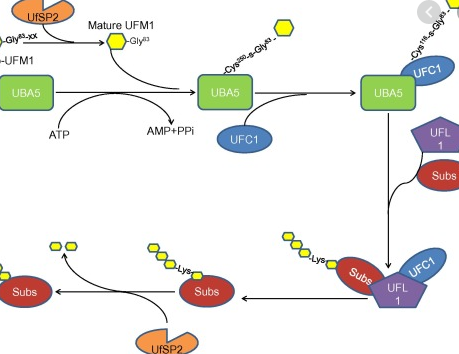
Un percorso chiamato “ufmilazione”: in questo percorso, un polipeptide chiamato Ufm1 è noto per colpire altre proteine, connettersi ad esse e modificarne la funzione. Una di queste proteine è l’Ufbp1, una proteina essenziale per le cellule immunitarie chiamate cellule B naive per diventare plasmacellule che producono anticorpi e per intensificare la produzione di anticorpi protettivi. “Comprendere meglio come funziona questo meccanismo di protezione naturale contribuirà alla progettazione di vaccini migliori”, scrivono i ricercatori. In effetti, gli attuali vaccini aiutano le cellule B ad avviare la memoria di alcuni invasori patogeni, consentendo una risposta immunitaria più efficace e più rapida.
L’aumento selettivo del percorso di ufilazione potrebbe, ad esempio, portare a un attacco più mirato del virus dell’influenza;
in caso di allergie, un intervento selettivo potrebbe, al contrario, bloccare la produzione di anticorpi contro gli allergeni;
per trattare malattie autoimmuni, come il lupus e l’artrite, manipolando questo stesso percorso, sarebbe possibile ridurre drasticamente i livelli di anticorpi che il corpo produce contro se stesso. Gli scienziati stanno già considerando di testare un modello di topo lupus.
Quale processo? Lo studio mostra che Ufbp1 sopprime l’enzima PERK per aiutare le cellule B a differenziarsi. Le proteine devono essere opportunamente ripiegate affinché si verifichino tutte le funzioni cellulari o corporee e PERK fa parte della naturale “risposta proteica spiegata” del corpo. PERK promuove quindi la risoluzione di problemi relativi a proteine ripiegate in modo improprio che non funzionano correttamente e possono diventare tossiche per le cellule: quando le proteine prodotte si piegano in modo inappropriato, viene attivato PERK, che interrompe la produzione di nuove proteine e riduce il numero di proteine ripiegate male.
Ma a questo punto, gli scienziati dimostrano che Ufbp1 sopprime PERK per garantire una produzione sufficiente di plasmacellule. Pertanto, quando c’è un deficit di Ufbp1 nelle cellule B, scoprono che, anche se le cellule B sopravvivono, lo sviluppo delle plasmacellule è compromesso. All’interno delle plasmacellule, Ufbp1 è sovraregolato, in modo che il reticolo endoplasmatico, che è la base dell’impianto di produzione di una cellula, possa espandersi e la capacità di piegare le proteine possono anche aumentare. Al contrario, i ricercatori dimostrano che un deficit di Ufbp1 nelle plasmacellule ostacola l’espansione del reticolo endoplasmatico e la produzione di anticorpi.
In sintesi, il percorso di ufilazione è un percorso essenziale per la produzione di cellule che secernono molte proteine, come le plasmacellule. Gli anticorpi funzionano come missili a lungo raggio e le plasmacellule solitamente li estraggono dal midollo osseo. Anche le cellule B sono prodotte nel e dal midollo osseo, ma circolano anche alla ricerca di invasori. Quando ne individuano uno, devono andare nella milza o in un linfonodo vicino per diventare una cellula del plasma. Le plasmacellule ritornano quindi nel midollo osseo. La sopravvivenza e il mantenimento delle plasmacellule è un equilibrio continuo e delicato, che può diventare fatale se qualcosa va storto. Senza questo equilibrio, le plasmacellule possono sfuggire al controllo, diventare cancerose anziché protettive e causare mieloma multiplo. Tra i molti passi avanti per gli scienziati, uno sarà determinare se il targeting per Ufbp1 è la soluzione per progettare la prossima generazione di trattamenti per mieloma multiplo.
Alcune persone nascono con l’assenza di alcuni componenti chiave del percorso di ufilazione e se l’impatto di questa carenza rimane scarsamente compreso, sappiamo che può provocare encefalopatia o disturbi del sangue. Il cattivo ripiegamento delle proteine è anche un fattore noto in condizioni come il morbo di Parkinson e il morbo di Alzheimer.
